《原子的结构》物质构成的奥秘PPT课件2
![]() 0
0
 《原子的结构》物质构成的奥秘PPT课件2
《原子的结构》物质构成的奥秘PPT课件2
一、学习目的:
1.能说出构成原子的各种粒子及带电情况。(重点)
2.知道相对原子质量表示的意义,会查相对原子质量表。(难点)
卢瑟福得出结论:
①原子核很小,原子内部有很大的空间
②原子中心有个带正电荷的原子核,α粒子途径金原子核附近受到斥力改变了运动方向;
③原子核质量比α粒子大,α粒子碰撞到原子核是被弹了回来
... ... ...
二、自主学习:
知识点一:原子的结构发现史
卢瑟福实验得出结论:
①原子核很_____,原子内部有很_____的空间
②原子中心有个带_____电荷的原子核,α粒子途径金原子核附近受到斥力改变了运动方向;
③原子核质量比α粒子_____,α粒子碰撞到原子核是被弹了回来
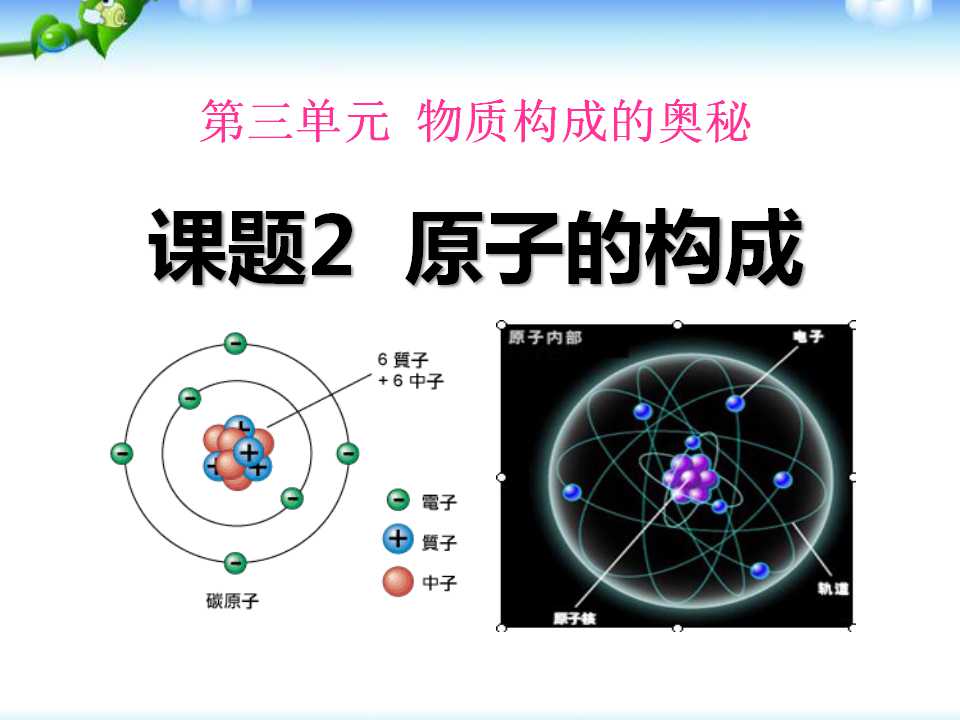
知识点二:原子的构成
1.由于原子是__________的最小粒子,所以原子在__________中不可以再分。但结构上原子是_____(填“可以”或“不可以”)再分的,原子是由居于原子中心的带_____电的_____和核外带_____电的_____构成。原子核是由_____和_____两种粒子构成的,中子_____显电性。
2.由于原子核内的质子带正电荷,所以原子核带正电,所带的正电荷数(即_____)与核外的_____相等,但电性相反,因此原子_____电性。不同种类的原子,核内的_____不同,核外的_____也不同。
... ... ...
三、合作探究:
探究一:原子的构成
1、分析讨论课本P53表3-1,你能发现哪些规律?
①原子中:质子数=核电荷数=核外电子数;
②原子一定有质子、电子,但不一定有中子(氢原子没有中子);
③质子数不一定等于中子数;
④不同的原子,质子数不同,核外电子数也不同。
2、你能总结出原子的结构吗?
... ... ...
探究二:相对原子质量
1.如何求某原子的相对原子质量?
(1)定义法:Ar=一个某原子的质量/一种碳-12原子的质量×1M12
(2)近似求法:Ar≈质子数+中子数
2.已知作为相对原子质量基准的一种碳原子的质量为1.993×10-26 kg,
(1)若一个铝原子的质量为4.482×10-26 kg,则铝原子的相对原子质量约为______。
(2)若氧原子的相对原子质量为16,则一个氧原子的质量为____________。
3.我国著名化学家张青莲教授与另一位科学家合作,测定了铟元素的相对原子质量新值。铟元素的核电荷数为49,相对原子质量为115。铟原子的中子数为( )
A.115 B.49 C.66 D.164
... ... ...
五、课堂练习:
1.已知原子的核电荷数,可以确定它的( )
(A)原子量 (B)质子数
(C)中子数 (D)电子数
2.原子(普通的氢除外)的原子核是( )
(A)由电子和质子构成
(B)由质子和中子构成
(C)由电子和中子构成
(D)不能再分
3.碳和镁的相对原子质量分别是12和24,则碳和镁的原子质量之比为( )
A.12:1 B.2:12 C.2:1 D.1:2
《原子的结构》物质构成的奥秘PPT课件6 复习提问 1.分子和原子的定义? 2.分子和原子的特征? 3.化学反应的实质? 在化学反应里分子可以分为原子,原子不能再分,那么用其它方法能不..
《原子的结构》物质构成的奥秘PPT课件5 学习目标 1、了解原子的结构,知道原子的微观构成。 2、了解原子核外电子的排布,知道离子的形成过程。 3、知道相对原子质量的概念和计算公式..
《原子的结构》物质构成的奥秘PPT课件4 观察表格(表4-2),思考下列问题 1、不同种原子之间有哪些区别? 不同原子的质子数、中子、电子数都不同。 2、所有原子都是由质子、中子、电..













 关于我们
关于我们 备案号:冀ICP备18037400号-20
备案号:冀ICP备18037400号-20